“类推”是常用的学习方法,但有时会产生错误结论。下列类推的结论中,正确的是( )
AⅣA族元素氢化物沸点顺序是GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是AsH3>PH3>NH3
B第二周期元素氢化物稳定性顺序是HF>H2O>NH3;则第三周期元素氢化物稳定性顺序也是HCl>H2S>PH3
C晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子
D干冰(CO2)是分子晶体;则二氧化硫(SO2)也是分子晶体
相关标签: 氢化物

《化妆品卫生规范》中规定的砷的测定方法是
A、分光光度法
B、氢化物原子吸收法
C、氢化物原子荧光光度法
D、二乙氨基二硫代甲酸银分光光度法
E、砷斑法
下列说法正确的是()。
A.稀有气体单质由原子组成,所以它们在固态时形成原子晶体
B.常温下是气体的物质,在固态时都是分子晶体,所以熔、沸点都较低
C.同族元素的共价型氢化物,其相对分子量愈大,分子间相互作用力愈小
D.同族元素的共价型氢化物,其相对分子量愈大,分子间相互作用力愈大
下表是元素周期表的一部分:
周期 族
IA
IIA
IIIA
IVA
V A
VIA
VIIA
2
②
③
④
⑤
⑥
3
⑦
⑧
⑨
⑩
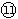

(1)表中元素⑩的氢化物的化学式为_____,此氢化物的还原性比元素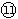 的氢化物的还原性____稳定性 (填强或弱)(2)某元素的原子结构示意图为:
的氢化物的还原性____稳定性 (填强或弱)(2)某元素的原子结构示意图为: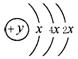 ,在周期表位于 。该氢化物沸点比甲烷 (填高或低)。(3)用电子式表示
,在周期表位于 。该氢化物沸点比甲烷 (填高或低)。(3)用电子式表示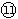 与⑧形成化合物形成过程: 。(4)写出⑦与⑨、⑨与
与⑧形成化合物形成过程: 。(4)写出⑦与⑨、⑨与 的最高价氧化物对应水化物反应的离子方程式:⑦与⑨: 、⑨与
的最高价氧化物对应水化物反应的离子方程式:⑦与⑨: 、⑨与 。
。
某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断()。
A.R一定是第四周期元素
B.R一定是ⅣA族元素
C.R的气态氢化物比同周期其他元素气态氢化物稳定
D.R气态氢化物的化学式为H2R
