追踪科学家的足迹 材料1:纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程: (1)20℃时,向浓氨水中通入足量的二氧化碳得到NH4HCO3饱和溶液; ②向NH4HCO3饱和溶液中加入食盐细粒,并不断搅拌,直到NaHCO3结晶析出完毕; ③将析出的晶体过滤,得到晶体和滤液,洗涤晶体,然后将晶体放在试管中充分加热,得到Na2CO3; ④向③的滤液中加入食盐细粒,析出NH4CI晶体,过滤,得到NH4CI. 材料2:四种盐在不同温度下的溶解度表.
温度 盐 溶解度
10℃
20℃
30℃
40℃
50℃
NaCl
35.8
36.0
36.3
36.6
37.0
NH4HCO3
15.8
21.0
27.0
------
------
NaHCO3
8.1
9.6
11.1
12.7
----
NH4Cl
33.3
37.2
41.4
45.8
50.4试回答下列问题:
(1)在实验室中,你选择的制备C02反应的化学方程式为___\_.在工业生产中,要获得生产纯碱的原料CO2你认为最经济实用的方法是以___\_为原料,该反应的化学方程式为______. (2)有人认为侯氏制碱法有以下优点,你认为其中正确的是______. A.生产过程中部分反应产物可作为原料循环使用 B.副产品是一种氮肥 C.反应都不需要加热,可节约能源 (3)检验③中的白色粉末中是否含有氯化钠的方法是______. (4)在②中,随着食盐的逐渐加入,溶液变成了NH4HCO3和NaCl的混合溶液,析出晶体之前,混合溶液中存在的离子有(用离子符号表示,下同.)___\_.在③中,将析出的晶体过滤后,溶液中数量减少的离子有___\_;滤液中仍然存在的离子有___\_.②中反应的化学方程式为______. (5)在20℃时,向含NH4HC0321g的饱和溶液中加入足量食盆.试通过计算说明,随着食盐的逐渐加入,为什么会有NaHC03晶体析出,而没有NH4Cl.
相关标签: 化学方程式

A~H都是初中化学中的常见物质,它们之间的转化关系如图所示.A是天然气的主要成分,E是一种常见的食品干燥剂.请回答
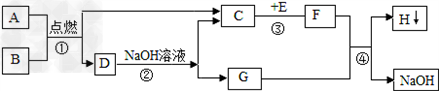
(1)A的化学式为 ;(2)反应③的基本反应类型是____ ;(3)反应②的化学方程式为 ;(4)反应④的化学方程式为 .
请仔细阅读下文,然后按要求写出有关反应的化学方程式:
食醋的主要成分是醋酸(化学式为CH3COOH ),其化学名称叫乙酸,是一种用途广泛的有机酸.通常情况下,纯净的乙酸是一种有强烈刺激性气味的无色液体,易溶于水和酒精.在水溶液中,乙酸只能解离出氢离子和乙酸根离子(CH3COO-);乙酸能跟活泼金属发生置换反应产生氢气,例如,跟锌反应的化学方程式可表示为:Zn+2CH3COOH═(CH3COO)2Zn+H2↑.
(1)请你写出醋酸分别跟氢氧化钠溶液、氧化铜反应的化学方程式;
(2)用化学方程式说明为什么家用的铝制器皿不宜用来盛放或烧煮食醋.
(3)铝是一种活泼金属,铝的化学性质较为特殊,它不但能跟盐酸反应生成三氯化铝和氢气,还能跟热的氢氧化钠水溶液起反应生成偏铝酸钠(NaAlO2)和氢气.请你写出该反应的化学方程式.
将CO2气体通入澄清的石灰水后溶液变浑浊,这是发生了____反应(填化学方程式).再继续通入CO2气体,液体又逐渐变清,发生反应的化学方程式是____,再把此透明溶液加热,又重新出现浑浊.此时发生反应的化学方程式是____.
