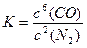题目
(14分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
SiO2+ C+ N2 Si3N4+ CO
Si3N4+ CO
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应中的氧化剂是____\_,其还原产物是___________;
(3)该反应的平衡常数表达式为K=_______;
(4)若知上述反应为放热反应,则其反应热ΔH_____\__零(填“大于”“小于”或“等于”);升高温度,其平衡常数值_______(填“增大”“减小”或“不变”);
(5)若使压强增大,则上述平衡向_______反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)="18"mol·(L·min)-1,
则N2消耗速率为v(N2)=_______mol·(L·min)-1。
相关标签: 氮化硅 化学方程式
提示:未搜索到的试题可在搜索页快速提交,您可在会员中心"提交的题"快速查看答案。
答案
查看答案

搜题

 Si3N4+6CO,有关说法不正确的是 ()
Si3N4+6CO,有关说法不正确的是 ()