题目
下列事实,不能用勒夏特列原理解释的是
A.氯水中有下列平衡:Cl2+H2O HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g) H2(g)+I2(g),平衡体系增大压强可使颜色变深
H2(g)+I2(g),平衡体系增大压强可使颜色变深
C.反应CO+NO2 CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
D.合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施(N2+3H2 2NH3;DH<0)
2NH3;DH<0)
相关标签: 逆反应
提示:未搜索到的试题可在搜索页快速提交,您可在会员中心"提交的题"快速查看答案。
答案
查看答案

搜题
相关试题
在一定条件下,反应3A(g)+B 2C+2D达到平衡
2C+2D达到平衡
(1)若升高温度,平衡向正反应方向移动,则逆反应是____\_(填“吸热”或“放热”)反应,逆反应速率________(填“增大”或“不变”或“变小”)
(2)若增加或减少B时,平衡不移动,则B是______态。
(3)若增大压强,平衡向逆反应方向移动,则可判断:B是_\__态,C是___态,D是__态
达到平衡后,将气体混合物的温度降低,下列叙述中正确的是()。
A.正反应速率加大,逆反应速率变小,平衡向正反应方向移动B.正反应速率变小,逆反应速率加大,平衡向逆反应方向移动C.正反应速率和逆反应速率都变小,平衡向正反应方向移动D.正反应速率和逆反应速率都变小,平衡向逆反应方向移动
A.正反应速率加大,逆反应速率变小,平衡向正反应方向移动B.正反应速率变小,逆反应速率加大,平衡向逆反应方向移动C.正反应速率和逆反应速率都变小,平衡向正反应方向移动D.正反应速率和逆反应速率都变小,平衡向逆反应方向移动
在固定容积的密闭容器中合成氨的反应达到了平衡,容器中含有0.1molN2、0.3molH2、0.1molNH3,若维持原来的条件,向该容器中再加入0.1molN2、0.3molH2、0.1molNH3,则( )
A.正、逆反应速率同时增大,平衡不移动
B.正、逆反应速率同时增大,NH3的百分含量升高
C.正、逆反应速率同时增大,平衡向逆反应方向移动
D.正、逆反应速率不变,平衡不移动
图为一带可移动隔板的密闭容器,某温度下,左、右两侧反应均达平衡,此时隔板处于容器中央。若保持温度不变,向左侧容器中充入一定量的H2,下列说法正确的是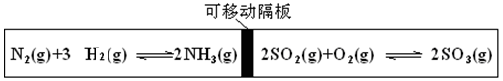
A.两侧平衡均向正反应方向移动
B.左侧平衡向逆反应方向移动
C.右侧平衡向逆反应方向移动
D.两侧平衡均向逆反应方向移动
